Antikörper-Effektormechanismen I: Neutralisierung und Komplementaktivierung
Antikörper erkennen nicht nur Antigene, sie lösen auch gezielte Abwehrreaktionen aus. Dieser Artikel beschreibt die ersten beiden zentralen Effektormechanismen: die Neutralisierung von Toxinen und Viren sowie die antikörpervermittelte Aktivierung des Komplementsystems. Beide Mechanismen zeigen, wie die spezifische Erkennung durch Antikörper mit der zerstörerischen Kraft anderer Immunkomponenten verknüpft wird.
Wie Antikörper Toxine neutralisieren
Bakterielle Toxine binden an spezifische Rezeptoren auf der Zelloberfläche. Diese Rezeptoren sind normalerweise für andere Zwecke vorgesehen, werden aber von den Toxinen als Eintrittspforte missbraucht. Die Bindung ist hochspezifisch. Im nächsten Schritt wird der Toxin-Rezeptor-Komplex durch Endozytose in die Zelle aufgenommen. Die anschließende Ansäuerung des Endosoms löst eine Konformationsänderung im Toxin aus: Der giftige Teil gelangt ins Zytoplasma und entfaltet dort seine zerstörerische Wirkung.
Wenn jedoch Antikörper – meist IgG – vorhanden sind, wird dieser Prozess frühzeitig unterbrochen. Die Antikörper binden an das Toxin und blockieren dessen Bindungsstellen, noch bevor es an Zellrezeptoren andocken kann. Ein mit Antikörpern bedecktes Toxin ist funktionsunfähig – neutralisiert. Die entstehenden Toxin-Antikörper-Komplexe werden von Makrophagen aufgenommen und abgebaut, ohne Schaden anzurichten.
Dieser Mechanismus ist besonders wichtig bei Erkrankungen, die hauptsächlich durch Toxine verursacht werden: Tetanus, Diphtherie und Botulismus. Impfungen gegen diese Krankheiten zielen darauf ab, neutralisierende Antikörper zu induzieren, die im Ernstfall sofort verfügbar sind.
Wie Antikörper Virusinfektionen verhindern
Viren binden über ihre Oberflächenproteine an spezifische Rezeptoren auf Körperzellen. Jeder Virustyp hat seine bevorzugten Rezeptoren: Influenzaviren erkennen Sialinsäure, HIV bindet an CD4 und Korezeptoren, Coronaviren nutzen ACE2. Nach der Bindung wird das Virus durch rezeptorvermittelte Endozytose aufgenommen; die Ansäuerung des Endosoms löst eine Konformationsänderung in den viralen Hüllproteinen aus, die die Fusion mit der Endosomenmembran ermöglicht und so die virale Nukleinsäure ins Zytoplasma entlässt.
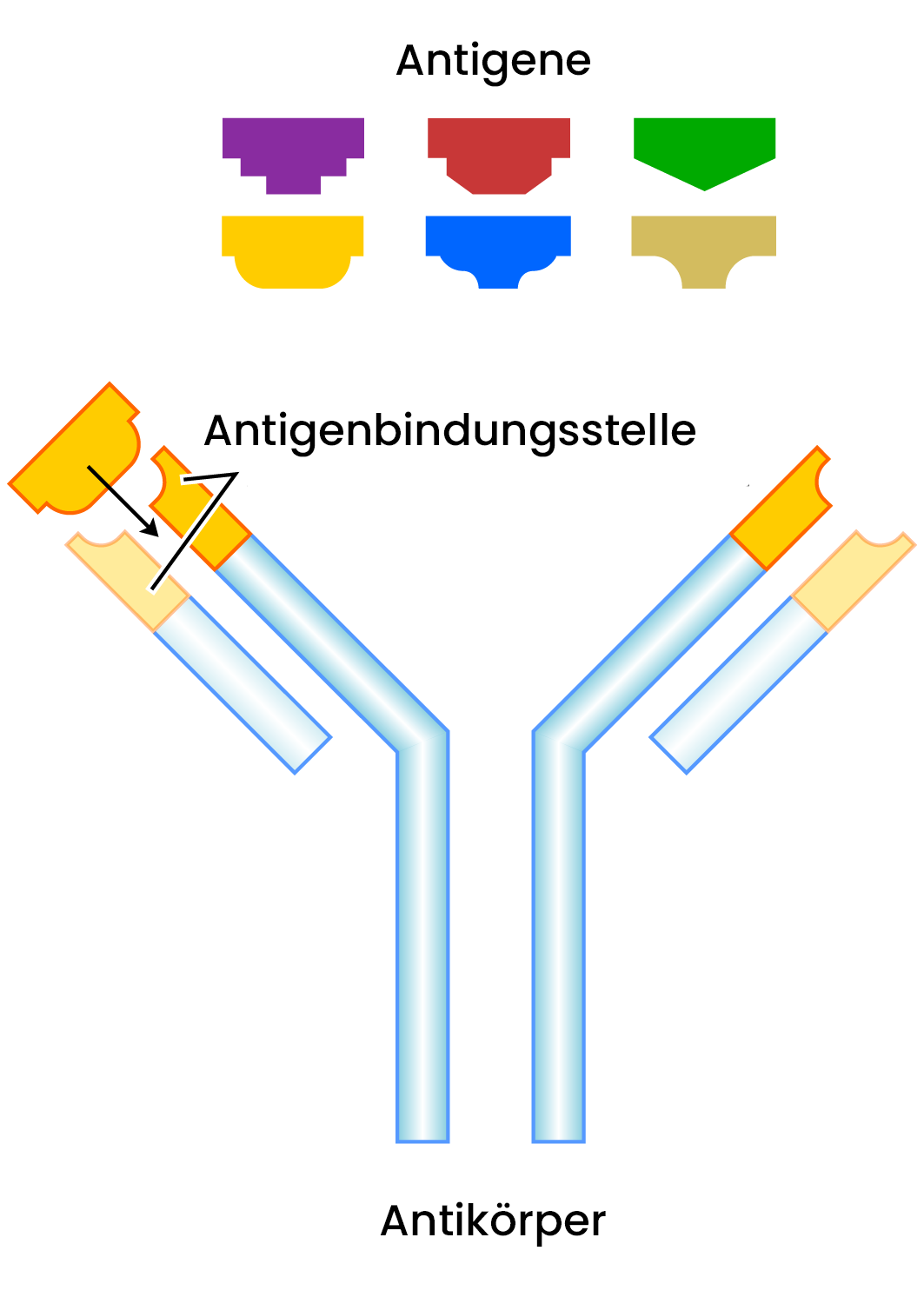
Neutralisierende Antikörper können diesen Prozess an mehreren Stellen blockieren. Am effektivsten ist die Blockierung der Rezeptorbindung: Antikörper, die an die Rezeptorbindungsstelle des Virus binden, wirken wie eine physische Blockade – das Virus kann nicht mehr andocken. Einige Antikörper verhindern auch die Fusion selbst, auch wenn das Virus bereits internalisiert wurde. Sie stabilisieren die virale Hülle in einer Konformation, die die Membranfusion verhindert; das Virus bleibt im Endosom gefangen und wird abgebaut.
Ein mit neutralisierenden Antikörpern bedecktes Virus ist infektionsunfähig. Dieses Prinzip liegt den meisten Impfungen gegen Viruserkrankungen zugrunde: Sie induzieren neutralisierende Antikörper, die eine Infektion von vornherein verhindern.
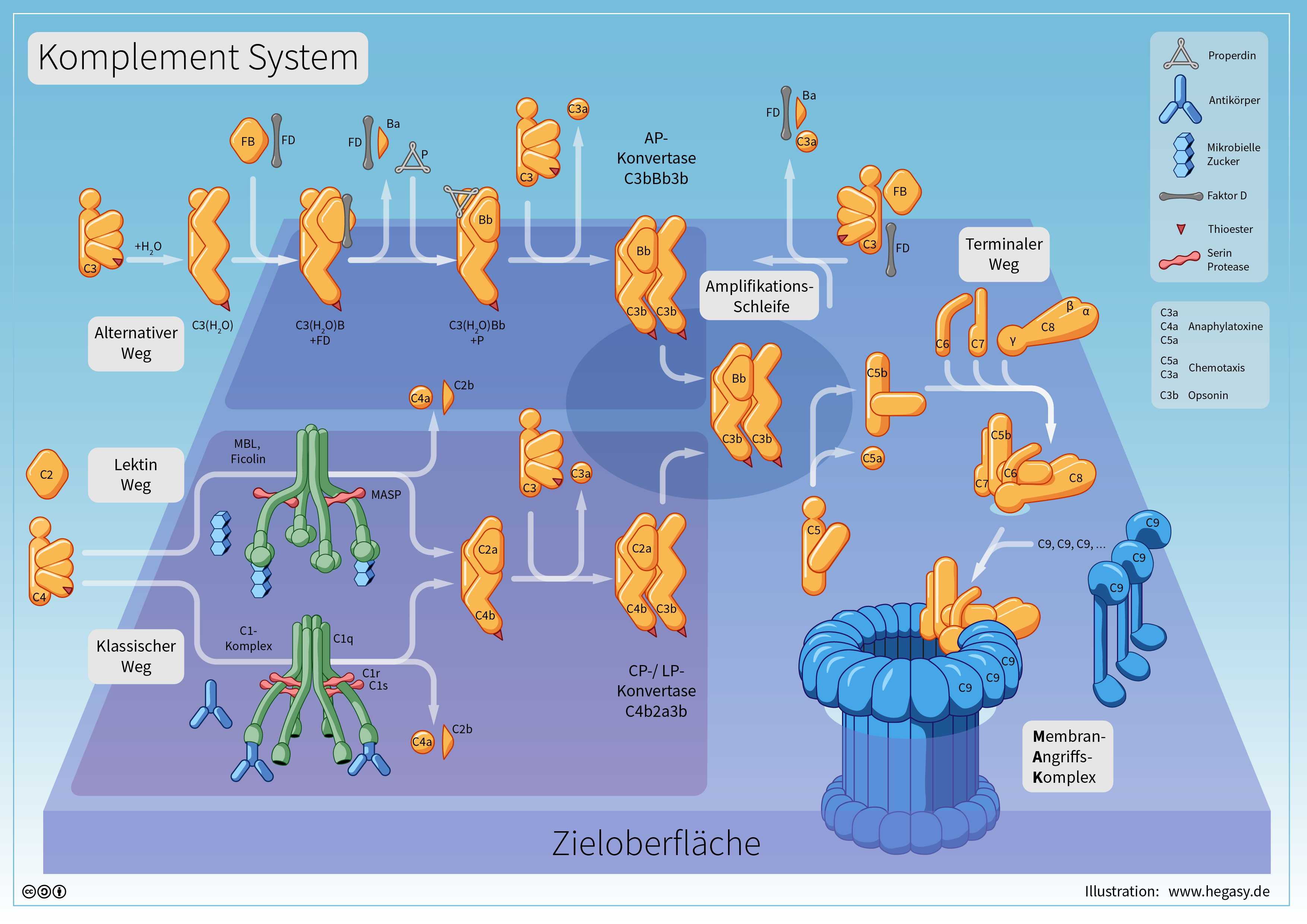
Die Komplementaktivierung durch Antikörper: Der klassische Weg
Die antikörpervermittelte Aktivierung des Komplementsystems ist ein eindrucksvolles Beispiel für die Zusammenarbeit von angeborener und erworbener Immunität: Die Antikörper liefern die Spezifität, das Komplementsystem die Zerstörungskraft.
Wenn pentamere IgM-Moleküle an Antigene auf einer Bakterienoberfläche binden, nehmen sie eine charakteristische „Krampenform" an. In dieser Konformation werden Bindungsstellen für C1q – das erste Protein des klassischen Wegs – zugänglich. Ein einziges gebundenes IgM-Molekül reicht aus, um C1q zu binden und die gesamte Kaskade zu starten. Diese extreme Effizienz macht IgM zum potentesten Komplementaktivator.
Auch IgG-Moleküle können das Komplementsystem aktivieren, benötigen dafür aber eine höhere Dichte auf der Oberfläche: C1q muss mindestens zwei nahe beieinander liegende IgG-Moleküle binden. Die C1q-Bindung an die Fc-Teile der Antikörper aktiviert C1r, das wiederum die Serinprotease C1s spaltet.
Die aktivierte C1s spaltet C4 und C2; die Bruchstücke C4b und C2a heften sich an die Bakterienoberfläche und bilden gemeinsam die C3-Konvertase. Diese ist der zentrale Verstärkungsschritt: Eine einzige Konvertase kann hunderte C3-Moleküle spalten. Das Spaltprodukt C3b lagert sich massenhaft an die Bakterienoberfläche und markiert das Bakterium für die Phagozytose. Gleichzeitig wirkt C3a als Entzündungsmediator und lockt weitere Immunzellen an.
Wenn C3b sich an die C3-Konvertase anheftet, entsteht die C5-Konvertase, die C5 spaltet. C5b rekrutiert C6, C7, C8 und mehrere C9-Moleküle und bildet so den Membranangriffskomplex (MAK). Dieser bohrt Poren in die Bakterienmembran: Wasser strömt ein, die Bakterien schwellen an und platzen. Der Mechanismus ist besonders effektiv gegen gramnegative Bakterien mit ihrer dünneren Zellwand.
Der klassische Weg verbindet damit die hochspezifische Erkennung durch Antikörper mit drei Wirkungen: Opsonierung durch C3b, Entzündungsförderung durch C3a und C5a, und direkte Lyse durch den MAK.