Antikörper-Effektormechanismen II: Opsonisierung, ADCC und IgA im Darm
Dieser Artikel beschreibt vier weitere zentrale Effektormechanismen von Antikörpern: die Opsonisierung und Phagozytose von Bakterien, die antikörpervermittelte Bekämpfung von Parasiten, die IgE-vermittelte Aktivierung von Mastzellen und ihre Bedeutung bei Allergien, sowie die einzigartige Rolle von IgA als stiller Wächter der Darmschleimhaut.
Opsonisierung und Phagozytose: Antikörper als Erkennungsmarker
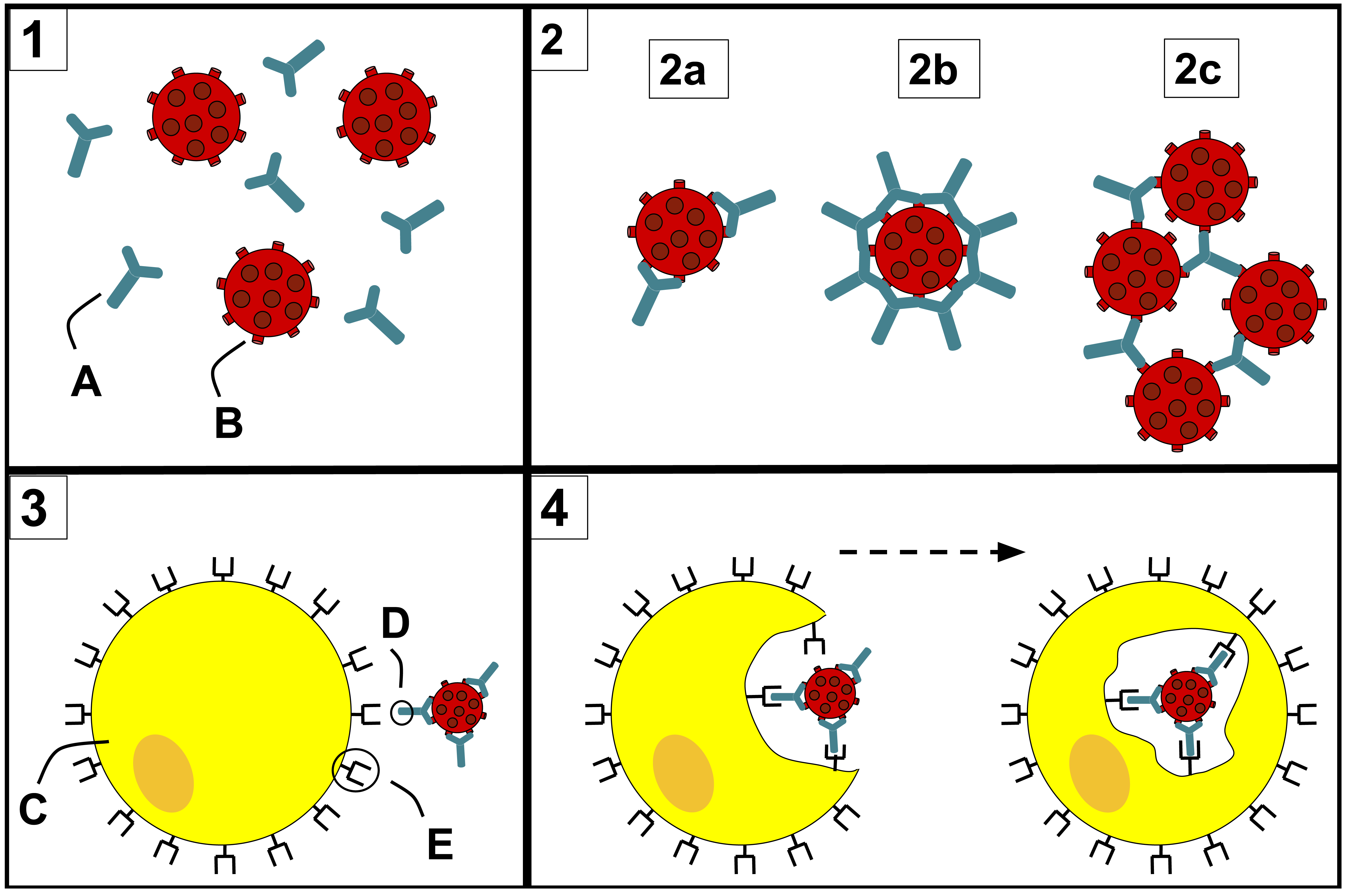
Opsonisierung – vom griechischen „opsonein" für „schmackhaft machen" – ist eine der wichtigsten Funktionen von Antikörpern bei der Bekämpfung bakterieller Infektionen. Ein Bakterium, das mit IgG-Antikörpern und dem Komplementfragment C3b bedeckt ist, wird von Makrophagen hundertfach effizienter erkannt und aufgenommen als ein unmarkiertes.
Makrophagen tragen zwei Typen von Erkennungsrezeptoren: Fc-Rezeptoren, die den Fc-Teil von Antikörpern binden, und Komplementrezeptoren (CR1), die C3b erkennen. Wenn ein Bakterium mit beiden Opsoninen bedeckt ist, binden beide Rezeptortypen gleichzeitig, was ein besonders starkes Phagozytosesignal erzeugt.
Die Abfolge ist präzise: Das opsonisierte Bakterium wird von Makrophagenmembranen umschlossen und in ein Phagosom verpackt. Lysosomen fusionieren mit dem Phagosom und setzen Verdauungsenzyme – Lipasen, Proteasen, Nukleasen – frei. Reaktive Sauerstoffspezies und Stickstoffmonoxid wirken zusätzlich bakterizid. Besonders wichtig ist Opsonisierung bei bekapselten Bakterien, die sich normalerweise durch ihre Polysaccharidkapsel vor Phagozytose schützen: Antikörper und Komplement können diese Schutzschicht überwinden.
Antikörper gegen Parasiten: Der ADCC-Mechanismus mit Eosinophilen
Bei der Abwehr großer Parasiten wie Helminthen (parasitische Würmer) stoßen klassische Phagozytose-Mechanismen an ihre Grenzen; ein Wurm ist schlicht zu groß, um von einem Makrophagen verschlungen zu werden. Das Immunsystem setzt daher auf einen anderen Mechanismus.
Eosinophile Granulozyten tragen Fc-Rezeptoren für IgE und IgG auf ihrer Oberfläche. Wenn IgE- und IgG-Antikörper an die Oberfläche eines Parasiten gebunden haben, erkennen Eosinophile diese Markierung über ihre Rezeptoren, binden an den antikörperbedeckten Parasiten und werden aktiviert. Sie degranulieren, setzen also den Inhalt ihrer Granula direkt auf die Parasitenoberfläche frei. Diese Granula enthalten hochgiftige Substanzen wie das Major Basic Protein, Eosinophil-Peroxidase und Eosinophil Cationic Protein, die die Kutikula des Wurms schädigen und bei massivem Angriff die Larve abtöten.
Dieser Prozess wird ebenfalls als antikörperabhängige zellvermittelte Zytotoxizität (ADCC) bezeichnet – strukturell ähnlich wie ADCC durch NK-Zellen, aber mit Eosinophilen als Effektorzellen.
Die Rolle von IgE: Parasitenabwehr und Allergien
IgE bindet mit sehr hoher Affinität über seinen Fc-Teil an den FcεRI-Rezeptor auf Mastzellen und basophilen Granulozyten. Eine ruhende Mastzelle ist so mit IgE-Molekülen besetzt und enthält Granula gefüllt mit Histamin und anderen Entzündungsmediatoren.
Wenn ein multivalentes Antigen – ein Antigen mit vielen gleichen Epitopen, wie es auf Parasitenoberflächen typisch ist – mehrere IgE-Moleküle auf der Mastzellmembran quervernetzt, löst dies ein Signal aus. Innerhalb von Sekunden beginnt die Mastzelle zu degranulieren: Histamin wird freigesetzt und bewirkt Gefäßerweiterung, erhöhte Gefäßpermeabilität und Kontraktion glatter Muskulatur. Zusätzlich synthetisiert die aktivierte Mastzelle Prostaglandine und Leukotriene, die die Entzündungsreaktion verstärken und verlängern. Leukotriene sind besonders potent bei der Bronchokonstriktion.
Bei einer parasitären Infektion ist diese Reaktion sinnvoll: Die Entzündung bringt mehr Immunzellen zum Infektionsort, und die Kontraktion glatter Muskulatur kann helfen, Darmparasiten auszustoßen. Bei einer Allergie gegen harmlose Substanzen wie Pollen oder Nahrungsmittel ist dieselbe Reaktion jedoch fehlgeleitet: Diesel selben Mechanismen, die zur Parasitenabwehr entstanden sind, verursachen nun die unangenehmen oder gefährlichen Symptome einer allergischen Reaktion, von Heuschnupfen bis zum anaphylaktischen Schock.
ADCC durch NK-Zellen: Brücke zwischen angeborener und adaptiver Immunität
NK-Zellen gehören zur angeborenen Immunität, können aber über Antikörper eng mit der adaptiven Immunität zusammenarbeiten. Sie tragen Fc-Rezeptoren (FcγRIII / CD16), die den Fc-Teil von IgG-Antikörpern binden.
Wenn IgG-Antikörper an Antigene auf der Oberfläche einer Zielzelle gebunden haben – etwa virale Proteine auf infizierten Zellen oder Tumorantigene auf Krebszellen – erkennt die NK-Zelle diese antikörperbedeckte Zielzelle. Die Quervernetzung ihrer Fc-Rezeptoren aktiviert die NK-Zelle, die daraufhin zytotoxische Granula mit Perforin und Granzyme freisetzt, die Apoptose der Zielzelle auslösen.
ADCC durch NK-Zellen ist besonders wichtig bei frühen Virusinfektionen, wenn virusinfizierte Zellen noch nicht genügend virale Peptide auf MHC-I präsentieren, um von zytotoxischen T-Zellen erkannt zu werden. Antikörper können jedoch virale Hüllproteine auf der Zelloberfläche erkennen und so NK-Zellen zur Zielzelle dirigieren. Dieses Prinzip nutzt auch die Krebsimmuntherapie: Therapeutische Antikörper wie Rituximab (gegen CD20 auf B-Zell-Lymphomen) und Trastuzumab (gegen HER2 auf Brustkrebszellen) wirken teilweise durch NK-Zell-Rekrutierung.
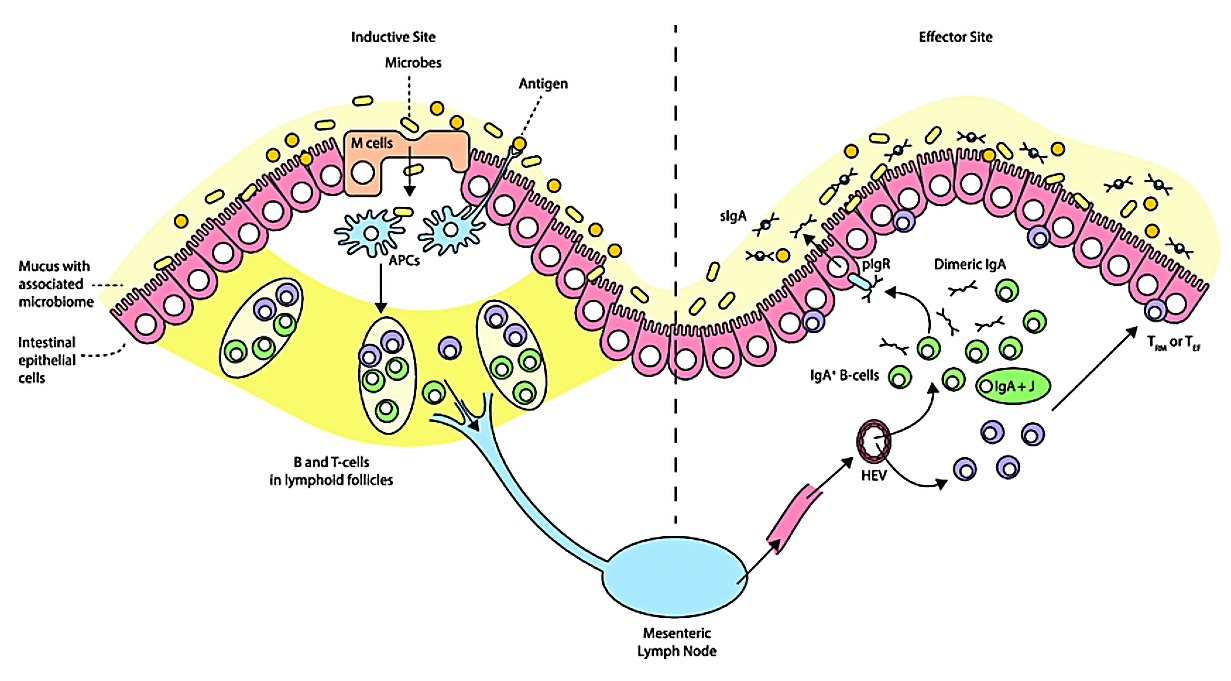
Die Bedeutung von IgA im Darm
Der Darm ist eine kritische Grenzfläche: Das Immunsystem kommt hier ständig mit Pathogenen, aber auch mit Billionen nützlicher Darmbakterien und harmlosen Nahrungsbestandteilen in Kontakt. IgA ist die Lösung für diese Herausforderung.
B-Zellen in der Lamina propria des Darms differenzieren zu IgA-produzierenden Plasmazellen, die IgA-Dimere mit J-Kette freisetzen. Diese Dimere binden an den polymeren Immunglobulin-Rezeptor (pIgR) auf der basolateralen Seite der Epithelzellen. Durch Transzytose werden sie durch die Epithelzelle transportiert. An der apikalen (luminalen) Seite wird der Rezeptor gespalten; ein Teil – die sekretorische Komponente – bleibt am IgA gebunden und schützt es vor proteolytischem Abbau durch Darmbakterienenzyme.
Das sekretorische IgA bindet an die Schleimschicht des Darmepithels und neutralisiert dort Pathogene und Toxine, noch bevor sie das Epithel erreichen. Es verhindert, dass Bakterien an Epithelzellen haften – eine Voraussetzung für viele Infektionen. Wichtig ist dabei: IgA aktiviert das Komplementsystem kaum und löst keine starken Entzündungsreaktionen aus. Dieser „stille Schutz" ist bewusst so angelegt, eine ständige Entzündung im Darm wäre schädlich für die wichtige symbiotische Darmflora.
Bei Neugeborenen ist die IgA-Produktion noch nicht vollständig entwickelt. Muttermilch enthält große Mengen IgA, das dem Kind in den ersten Lebensmonaten passiven Schutz bietet, bis das eigene Immunsystem ausgereift ist.