Antikörper – Struktur und Funktion
Antikörper – auch Immunglobuline genannt – sind die molekularen Waffen der humoralen Immunabwehr. Ihre charakteristische Y-Form ist kein Zufall, sondern das Ergebnis einer präzisen Arbeitsteilung: Die zwei Arme des Y erkennen Antigene hochspezifisch, der Stamm vermittelt die biologische Wirkung. Diese Trennung von Erkennung und Effektorfunktion macht Antikörper zu einem der vielseitigsten Moleküle des Immunsystems.
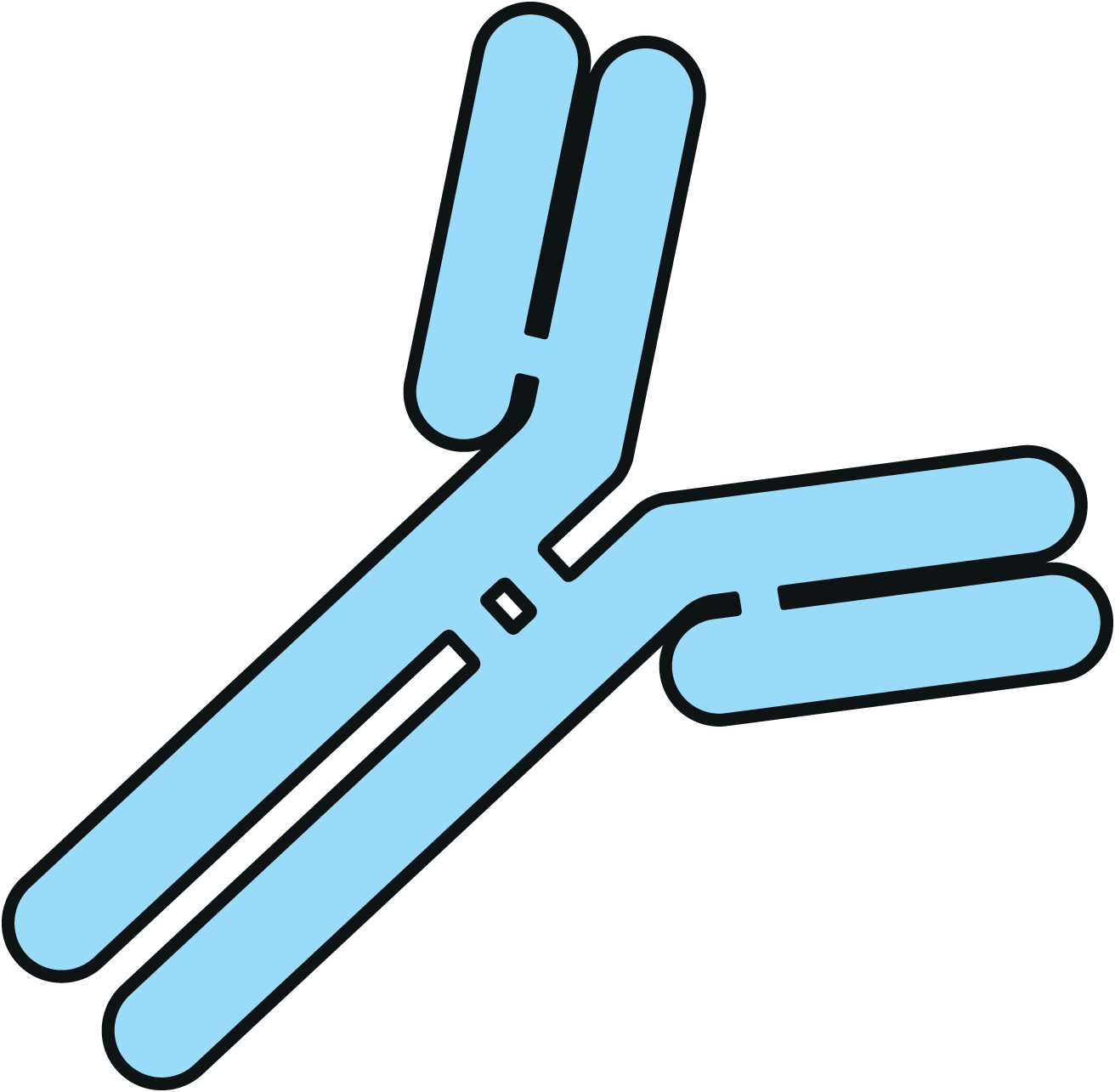
Immunglobuline: Struktur und molekulare Organisation
Antikörper bestehen aus vier Polypeptidketten: zwei identischen schweren Ketten und zwei identischen leichten Ketten, die durch Disulfidbrücken miteinander verbunden sind. Jeder Arm des Y enthält eine Antigenbindungsstelle, die sich in den variablen Regionen der schweren und leichten Ketten befindet. Jedes Antikörpermolekül kann damit zwei Antigenmoleküle gleichzeitig binden. Die variable Region ist bei verschiedenen Antikörpern unterschiedlich; sie bestimmt die Spezifität, also welches Antigen erkannt wird.
Der Stamm des Y besteht aus den konstanten Regionen der schweren Ketten und wird als Fc-Region bezeichnet. Sie bestimmt die Effektorfunktionen: wie effektiv das Komplementsystem aktiviert wird, an welche Fc-Rezeptoren auf Immunzellen der Antikörper bindet, und wie der Antikörper im Körper verteilt wird. Die zwei Arme des Y werden zusammen als Fab-Region (Fragment antigen binding) bezeichnet.
Die fünf Antikörperklassen
Immunglobulin G (IgG) ist mit etwa 70–75 % aller Antikörper im Blut die häufigste Klasse, unterteilt in vier Subklassen (IgG1–4) mit leicht unterschiedlichen Eigenschaften. Mit einer Halbwertszeit von 21–28 Tagen zirkuliert IgG besonders lang im Körper. Es ist klein genug, um aus dem Blut ins Gewebe zu diffundieren, und die einzige Antikörperklasse, die die Plazenta passieren kann – ungeborene Kinder werden so mit mütterlichen Antikörpern versorgt und in den ersten Lebensmonaten geschützt.
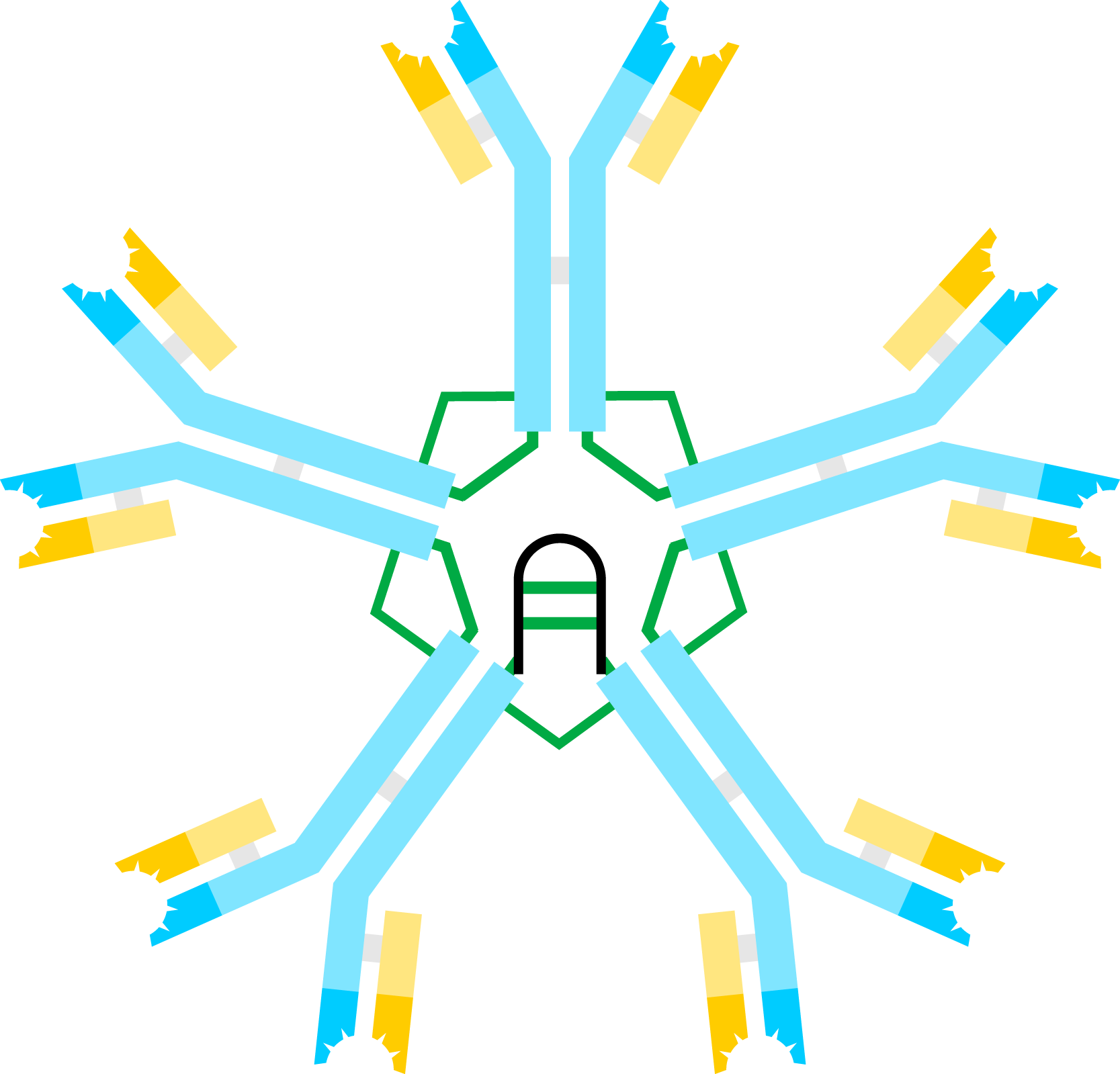
Immunglobulin M (IgM) ist ein Pentamer – fünf Y-förmige Einheiten, verbunden durch eine J-Kette. Mit seinen zehn Antigenbindungsstellen ist IgM besonders effektiv bei der Komplementaktivierung: Ein einziges gebundenes IgM-Molekül reicht aus, um C1q zu binden und die Kaskade zu starten. IgM ist der erste Antikörper der Primärantwort, hat aber mit sieben Tagen eine kürzere Halbwertszeit als IgG. Es bleibt wegen seiner Größe im Blutgefäßsystem.
Immunglobulin A (IgA) existiert im Blut als Monomer, in Körpersekreten jedoch als Dimer mit sekretorischer Komponente. Es ist der Hauptantikörper in Speichel, Tränen, Muttermilch und Schleimhautsekreten – also an den Eintrittspforten des Körpers. Es aktiviert das Komplementsystem kaum und löst keine starken Entzündungsreaktionen aus: ein „stiller Schutz", der Erreger neutralisiert, ohne die normale Flora zu stören.
Immunglobulin E (IgE) kommt normalerweise in minimalen Konzentrationen (3 × 10⁻⁵ mg/ml) im Blut vor und hat eine Halbwertszeit von nur zwei Tagen. Es bindet über seinen Fc-Teil mit hoher Affinität an Mastzellen und basophile Granulozyten. Bei Antigenkontakt werden diese Zellen aktiviert und setzen Histamin und andere Entzündungsmediatoren frei. Die eigentliche biologische Rolle von IgE ist die Abwehr von Parasiten, insbesondere Würmern. Bei Allergien ist dieselbe Reaktion gegen harmlose Substanzen jedoch fehlgeleitet.
Immunglobulin D (IgD) findet sich hauptsächlich als Rezeptor auf der Oberfläche naiver B-Zellen. Es macht nur etwa 0,3 % der Serum-Antikörper aus; seine genaue Funktion ist noch nicht vollständig geklärt, aber es scheint bei der B-Zell-Aktivierung eine Rolle zu spielen.
Funktionelle Spezialisierung der Isotypen
Die fünf Isotypen sind für unterschiedliche Aufgaben spezialisiert. Bei der Neutralisierung von Toxinen und Viren sind alle IgG-Subklassen sowie IgA sehr effektiv. Bei der Opsonisierung für die Phagozytose dominiert IgG1, gefolgt von IgG3. Die Aktivierung von NK-Zellen (ADCC) wird hauptsächlich von IgG1 und IgG3 vermittelt. Die Sensibilisierung von Mastzellen ist nahezu exklusiv Aufgabe von IgE. Die Komplementaktivierung über den klassischen Weg wird am stärksten durch IgM ausgelöst, gefolgt von IgG1 und IgG3. Nur IgA kann effizient durch Epithelien transportiert werden; nur IgG passiert die Plazenta; nur IgM bleibt wegen seiner Größe im Blutgefäßsystem.
Die mittleren Serumkonzentrationen spiegeln die relative Bedeutung wider: IgG1 liegt bei 9 mg/ml, IgG2 bei 3 mg/ml, IgA bei 2,1 mg/ml, IgM bei 1,5 mg/ml, IgG3 bei 1 mg/ml, IgG4 bei 0,5 mg/ml, IgD bei 0,04 mg/ml und IgE bei 3 × 10⁻⁵ mg/ml.