Makrophagen: Aktivierung, Akut-Phase-Reaktion und antigenpräsentierende Zellen
Makrophagen sind weit mehr als Fresszellen. Nach Erkennung eines Erregers werden sie zu aktiven Effektorzellen, die eine Kaskade lokaler und systemischer Reaktionen auslösen. Diese Reaktionen kulminieren in der Akut-Phase-Reaktion – einer koordinierten Antwort der Leber, die die antimikrobielle Abwehr des gesamten Organismus verstärkt. Am Ende dieser Kette stehen antigenpräsentierende Zellen, die die Brücke zur adaptiven Immunantwort schlagen.
Aktivierung von Makrophagen durch Pathogenkontakt
Die Bindung von Erregerstrukturen an Makrophagenrezeptoren initiiert eine koordinierte Aktivierungssequenz. Nach Rezeptorbindung werden Adapterproteine rekrutiert. Bei Toll-like-Rezeptoren führt dies zur Aktivierung von Signalwegen über MyD88 und TRIF, die letztendlich Transkriptionsfaktoren wie NF-κB aktivieren.
Die Signaltransduktion resultiert in der Expression und Freisetzung verschiedener Mediatoren: Proinflammatorische Zytokine wie TNF-α, IL-1 und IL-6 werden synthetisiert und sezerniert. TNF-α und IL-1 induzieren die Expression von Adhäsionsmolekülen auf Endothelzellen, erhöhen die Gefäßdurchlässigkeit und aktivieren weitere Immunzellen. IL-6 ist ein zentraler Mediator der Akut-Phase-Reaktion in der Leber.
Parallel werden inflammatorische Lipidmediatoren gebildet: Arachidonsäure wird aus Membranphospholipiden freigesetzt und zu Prostaglandinen und Leukotrienen metabolisiert, die vaskuläre Veränderungen der Entzündung verstärken und die Schmerzwahrnehmung beeinflussen. Chemokine wie IL-8, MCP-1 und MIP-1α etablieren Konzentrationsgradienten, die neutrophile Granulozyten, Monozyten und andere Leukozyten zum Infektionsort rekrutieren.
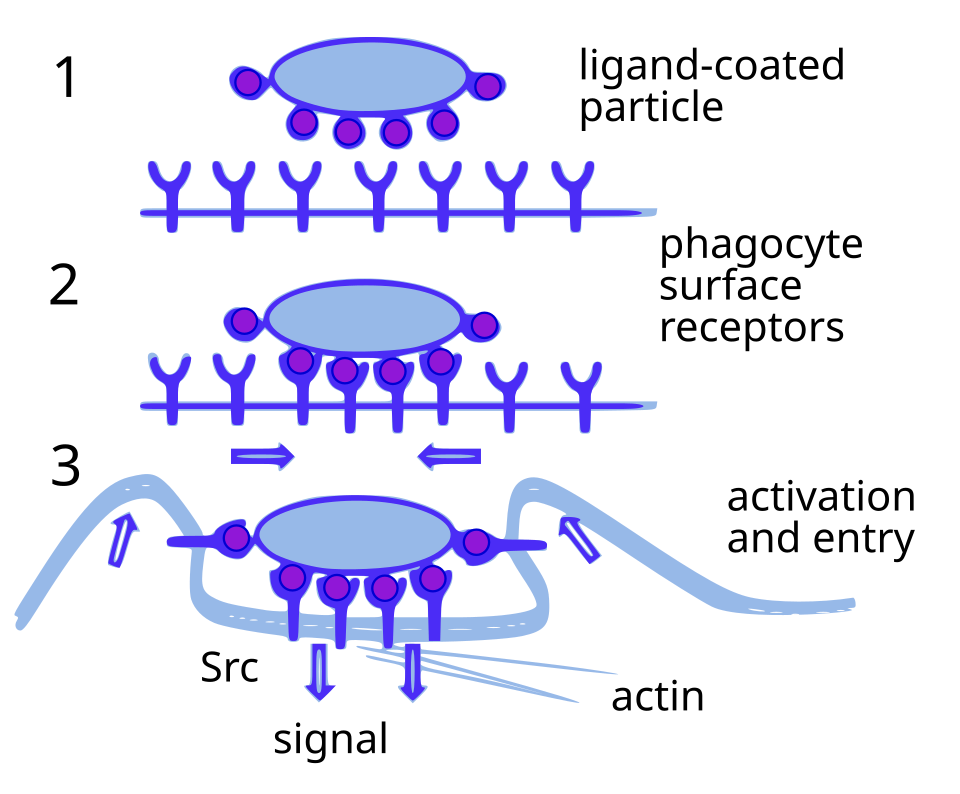
Die Phagozytose wird durch die Aktivierung ebenfalls verstärkt: Bakterien werden in ein Phagosom verpackt, das mit Lysosomen fusioniert. Im Phagolysosom bauen hydrolytische Enzyme die Bakterien ab. Gleichzeitig produziert die NADPH-Oxidase reaktive Sauerstoffspezies, und die Stickstoffmonoxid-Synthase generiert NO – beide Moleküle wirken direkt bakterizid. Zusätzlich exprimiert der aktivierte Makrophage mehr MHC-II-Moleküle und costimulatorische Moleküle, was die Antigenpräsentation und T-Zell-Aktivierung optimiert.
Systemische Akut-Phase-Reaktion
Die lokale Entzündung löst eine systemische Antwort aus: die Akut-Phase-Reaktion. Proinflammatorische Zytokine – insbesondere IL-6, IL-1 und TNF-α – gelangen über die Blutbahn zur Leber, wo sie in Hepatozyten Signalkaskaden aktivieren, die zur Produktion von Akut-Phase-Proteinen führen. Die Syntheserate dieser Proteine kann innerhalb von Stunden um das Hundertfache steigen.
C-reaktives Protein (CRP) liegt als zyklisches Pentamer aus fünf identischen Untereinheiten vor. Es bindet an Phosphocholin, eine Komponente bakterieller Membranen und apoptotischer Zellen, und markiert diese für Phagozytose (Opsonierung) sowie für die Aktivierung des Komplementsystems über den klassischen Weg. CRP hat keine Affinität zu Phosphocholin auf intakten körpereigenen Zellen – die Selektivität ist damit gewährleistet.
Mannosebindendes Lektin (MBL) gehört zur angeborenen Immunität, ist aber strukturell und funktionell Antikörpern ähnlich. Es bindet an Mannose- und N-Acetylglucosamin-Reste auf bakteriellen, viralen und Pilzoberflächen – Strukturen, die auf Säugetierzellen durch terminale Sialinsäuren maskiert sind. Nach Bindung aktiviert MBL das Komplementsystem über den Lektinweg.
Serumamyloid A (SAA) wird ebenfalls stark induziert. Es hat chemotaktische Aktivität für Phagozyten, moduliert die Zytokinproduktion und beeinflusst den Lipidstoffwechsel. Chronisch erhöhte SAA-Spiegel können zur Amyloidose führen. Fibrinogen wird vermehrt synthetisiert, erhöht die Blutviskosität – klinisch erkennbar an einer erhöhten Blutsenkungsgeschwindigkeit – und trägt zur Eindämmung von Infektionen durch Bildung von Fibrinnetzen bei.
Antigenpräsentierende Zellen: Drei spezialisierte Zelltypen
Als antigenpräsentierende Zellen (APC) werden Zellen bezeichnet, die mithilfe von MHC-II-Molekülen prozessierte Antigene auf ihrer Oberfläche präsentieren und dadurch CD4+ T-Zellen aktivieren können. Drei Zelltypen erfüllen diese Funktion mit unterschiedlichen Spezialisierungen.
Makrophagen sind professionelle Fresszellen, die überall in Geweben vorkommen. Sie nehmen Erreger, apoptotische Zellen und Zelltrümmer auf, verarbeiten sie und präsentieren Peptidfragmente auf MHC-II. Ihre Antigenpräsentation erfolgt primär in peripheren Geweben und dient der Aktivierung von Effektor-T-Zellen, die bereits durch vorherige Antigenkontakte sensibilisiert wurden.
Dendritische Zellen sind die potentesten antigenpräsentierenden Zellen und spezialisiert auf die Initiierung primärer Immunantworten. Im unreifen Zustand überwachen sie in peripheren Geweben kontinuierlich ihre Umgebung. Nach Antigenaufnahme und PAMP-Aktivierung durchlaufen sie einen Reifungsprozess: Sie reduzieren ihre phagozytische Aktivität, erhöhen die Expression von MHC-II und kostimulatorischen Molekülen (CD80, CD86) und wandern zu den drainierenden Lymphknoten. Dort präsentieren sie Antigene naiven T-Zellen; diese Fähigkeit, noch nie aktivierte T-Zellen anzusprechen, unterscheidet dendritische Zellen von allen anderen APCs.
B-Lymphozyten exprimieren antigenspezifische B-Zell-Rezeptoren auf ihrer Oberfläche. Bei Antigenbindung wird das Antigen aufgenommen, verarbeitet und auf MHC-II präsentiert. B-Zellen präsentieren typischerweise lösliche Proteinantigene, die sie hochaffin über ihre spezifischen Rezeptoren binden. Ihre Antigenpräsentation ist zentral für die T-Zell-abhängige Antikörperproduktion und die Bildung von Gedächtnis-B-Zellen.
Die drei APC-Typen sind in unterschiedlichen anatomischen Regionen der Lymphknoten lokalisiert: Dendritische Zellen in T-Zell-reichen Bereichen, B-Zellen in den Follikeln und Makrophagen in den Randbereichen.