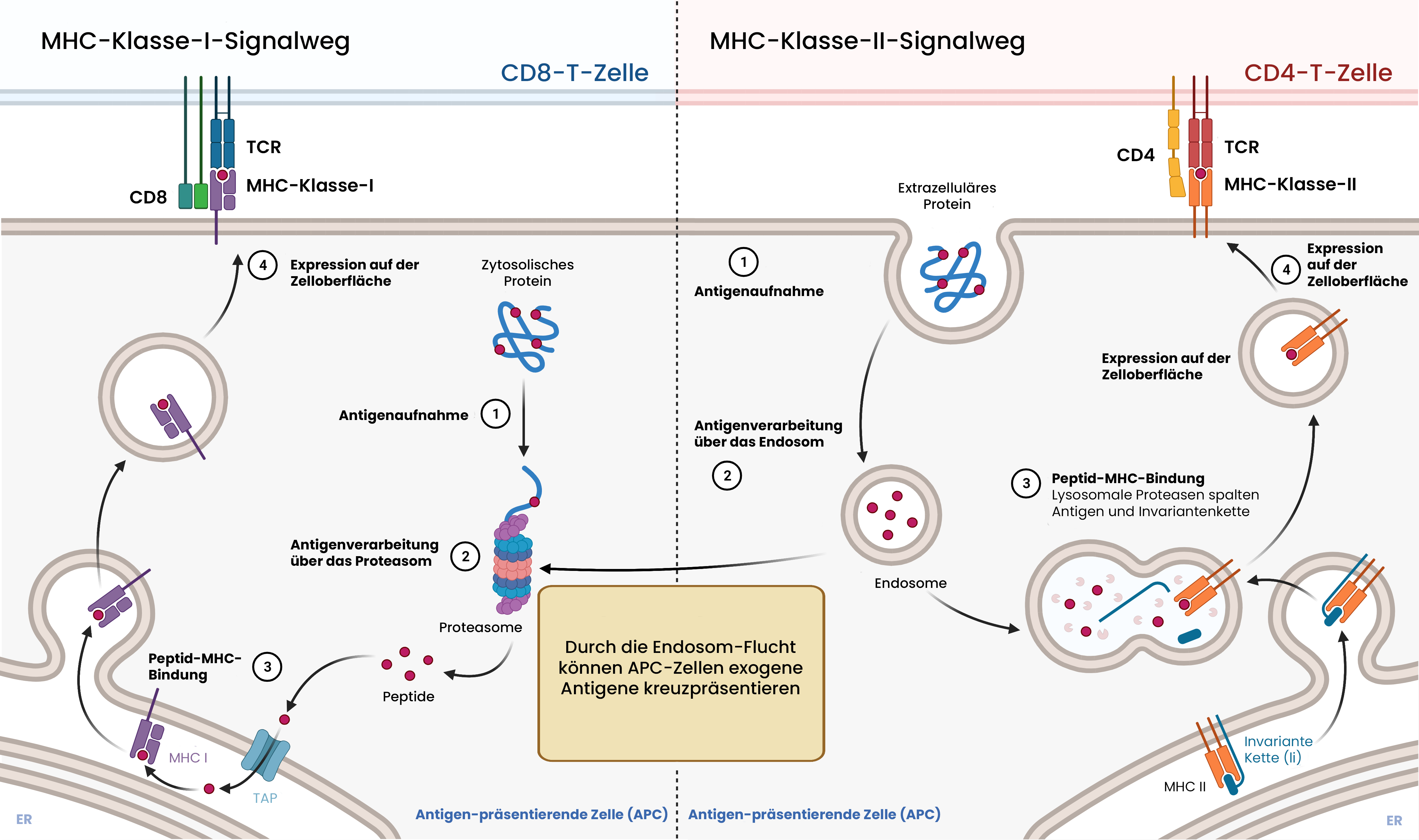
MHC-Moleküle und Antigenpräsentation
Ein zentrales Konzept für das Verständnis der T-Zell-Funktion ist das System der MHC-Moleküle (Major Histocompatibility Complex). Sie sind die molekularen Präsentationsplattformen des Immunsystems: Ohne sie können T-Zellen weder Infektionen erkennen noch eine Immunantwort koordinieren. Es gibt zwei Hauptklassen: MHC-Klasse-I und MHC-Klasse-II. Diese erfüllen grundlegend verschiedene Aufgaben und sprechenunterschiedliche T-Zell-Populationen an.
MHC-Moleküle: Struktur und Eigenschaften
MHC-Moleküle sind membranständige Glykoproteine, die Peptidfragmente binden und auf der Zelloberfläche präsentieren. Ihre Eigenschaften definieren die Regeln der T-Zell-Erkennung.
MHC-Moleküle binden ausschließlich Peptide – keine intakten Proteine, Kohlenhydrate oder Lipide. Ein einzelnes MHC-Molekül kann verschiedene Peptide binden, die ein gemeinsames Bindungsmotiv aufweisen. Diese breite Spezifität ermöglicht es der begrenzten Zahl verschiedener MHC-Moleküle eines Individuums, ein großes Peptidrepertoire zu präsentieren. MHC-Moleküle werden nur dann stabil auf der Zelloberfläche exprimiert, wenn sie mit einem Peptid beladen sind – eine Qualitätskontrolle, die sicherstellt, dass nur funktionelle Komplexe präsentiert werden.
MHC-I besteht aus einer polymorphen schweren Kette mit drei extrazellulären Domänen (α1, α2, α3) und β2-Mikroglobulin. Die Peptidbindungsgrube ist an beiden Enden geschlossen und bindet Peptide von 8 bis10 Aminosäuren. MHC-I-Moleküle werden auf praktisch allen kernhaltigen Zellen exprimiert – Erythrozyten tragen kein MHC-I, da sie keinen Zellkern besitzen.
MHC-II besteht aus zwei polymorphen Polypeptidketten (α und β). Die Peptidbindungsgrube ist an beiden Enden offen und bindet längere Peptide von 13–25 Aminosäuren. MHC-II-Moleküle finden sich primär auf professionellen antigenpräsentierenden Zellen, können aber auf anderen Zelltypen nach Stimulation mit Interferon-γ induziert werden.
Die polymorphen Regionen beider MHC-Klassen sind zwischen Individuen hochvariabel. Diese genetische Diversität ist evolutionär vorteilhaft: Unterschiedliche MHC-Varianten präsentieren verschiedene Peptidrepertoires, was auf Populationsebene die Wahrscheinlichkeit erhöht, dass zumindest einige Individuen Peptide neuer Erreger effektiv präsentieren können.
Prozessierungsweg MHC-Klasse I: Intrazelluläre Antigene
Dieser Weg präsentiert intrazelluläre Antigene und überwacht das Zytosol auf Virusinfektionen oder abweichende Proteinexpression. Proteine im Zytosol werden kontinuierlich durch das Proteasom abgebaut; für den Abbau bestimmte Proteine werden zuvor durch Ubiquitin-Konjugation markiert.
Die entstehenden Peptide werden durch den TAP-Transporter (Transporter associated with Antigen Processing) vom Zytosol ins endoplasmatische Retikulum transportiert. Dort lädt ein Peptid-Beladungskomplex, bestehend aus Calretikulin, ERp57, β2-Mikroglobulin und Tapasin, die Peptide auf neue MHC-I-Moleküle. Korrekt beladene Komplexe wandern über den Golgi-Apparat zur Zelloberfläche, wo sie CD8+-T-Zellen präsentiert werden.
Da praktisch alle kernhaltigen Zellen MHC-I tragen, kann jede infizierte Zelle durch diesen Mechanismus signalisieren: „Ich bin infiziert." Erscheinen auf der Oberfläche fremde Peptide statt körpereigener, schlägt das Immunsystem Alarm.
Prozessierungsweg MHC-Klasse II: Extrazelluläre Antigene
Dieser Weg dient der Präsentation extrazellulärer Antigene. Proteine aus der extrazellulären Umgebung werden durch Phagozytose, rezeptorvermittelte Endozytose oder Makropinozytose aufgenommen. Sie gelangen in Endosomen, die zunehmend ansäuern und mit Lysosomen fusionieren, wo Cathepsine und andere Proteasen die Proteine zu Peptidfragmenten zersetzen.
Parallel dazu werden MHC-II-Moleküle im endoplasmatischen Retikulum synthetisiert. Um vorzeitige Beladung mit endogenen Peptiden zu verhindern, ist die Peptidbindungsgrube durch die invariante Kette (Ii) blockiert, die die MHC-II-Moleküle zu spezialisierten Endosomen dirigiert. Dort wird die invariante Kette schrittweise abgebaut, bis nur noch das Fragment CLIP in der Bindungsgrube verbleibt. Das Chaperon HLA-DM katalysiert anschließend den Austausch von CLIP gegen hochaffine Peptide aus dem Antigenabbau. Die beladenen MHC-II-Peptid-Komplexe werden zur Zelloberfläche transportiert, wo sie CD4+-T-Zellen präsentiert werden.
Cross-Präsentation: Eine wichtige Ausnahme
Obwohl die beiden MHC-Prozessierungswege normalerweise strikt getrennt sind, existiert ein spezialisierter Mechanismus: die Cross-Präsentation. Dabei können dendritische Zellen extrazelluläre Antigene auf MHC-I präsentieren – also außerhalb des normalen Wegs.
Bei der Cross-Präsentation nehmen dendritische Zellen virusinfizierte apoptotische Zellen oder virusassoziierte Antigene auf. Teile dieser Antigene werden aus dem Endosom ins Zytosol exportiert, durch das Proteasom prozessiert und über TAP ins ER transportiert, wo sie auf MHC-I geladen werden. Dieser Mechanismus ist besonders wichtig bei Virusinfektionen, bei denen das Virus primär Nicht-APCs infiziert: Ohne Cross-Präsentation könnten keine zytotoxischen T-Zellen aktiviert werden, da diese ausschließlich auf MHC-I-präsentierte Antigene reagieren.