Molekulare Grundlagen
Eine elementare Fähigkeit des Immunsystems ist das Unterscheidenkönnen zwischen körpereigenen und körperfremden Strukturen. Diese Unterscheidung ist die Voraussetzung für jede Immunantwort: Nur wenn das System zuverlässig erkennt, was „fremd" ist, kann es gezielt reagieren, ohne gesundes Gewebe zu schädigen. Die Unterscheidung basiert auf mehreren molekularen Erkennungssystemen, die auf verschiedenen Ebenen zusammenarbeiten.
Molekulare Grundlagen der Selbst-Fremd-Erkennung
Pattern Recognition Receptors (PRR) sind genetisch festgelegte Rezeptoren, die pathogen-assoziierte molekulare Muster (PAMPs) erkennen. Diese PAMPs sind konservierte Strukturen, die auf Erregern vorkommen, bei körpereigenen Zellen jedoch fehlen oder nicht zugänglich sind. PRR ermöglichen eine schnelle Erkennung ohne vorherige Sensibilisierung. Ihre Spezifität ist breiter als die von Antikörpern oder T-Zell-Rezeptoren, erlaubt aber dennoch die Unterscheidung zwischen verschiedenen Erregerklassen. Die PAMPs sind evolutionär konserviert, weil sie essenziell für die Erregerbiologie sind und nicht ohne Fitnessverlust mutiert werden können.
MHC-Klasse-I-Moleküle befinden sich auf allen kernhaltigen Zellen und präsentieren kontinuierlich Peptide aus dem Zellinneren. Gesunde Zellen präsentieren körpereigene Peptide, die vom Immunsystem toleriert werden. Infizierte oder entartete Zellen präsentieren abweichende Peptide, die als fremd erkannt werden und eine Immunantwort auslösen. Dieses System ermöglicht die Überwachung des intrazellulären Raums.
MHC-Klasse-II-Moleküle finden sich vorwiegend auf antigenpräsentierenden Zellen. Sie präsentieren Peptide aus aufgenommenen extrazellulären Antigenen. Diese Präsentation ist essenziell für die Aktivierung der erworbenen Immunität und die Koordination zwischen angeborener und adaptiver Abwehr.
Die Kombination dieser Erkennungssysteme ermöglicht die Unterscheidung zwischen Selbst und Fremd auf molekularer Ebene – sowohl im extrazellulären als auch im intrazellulären Bereich.
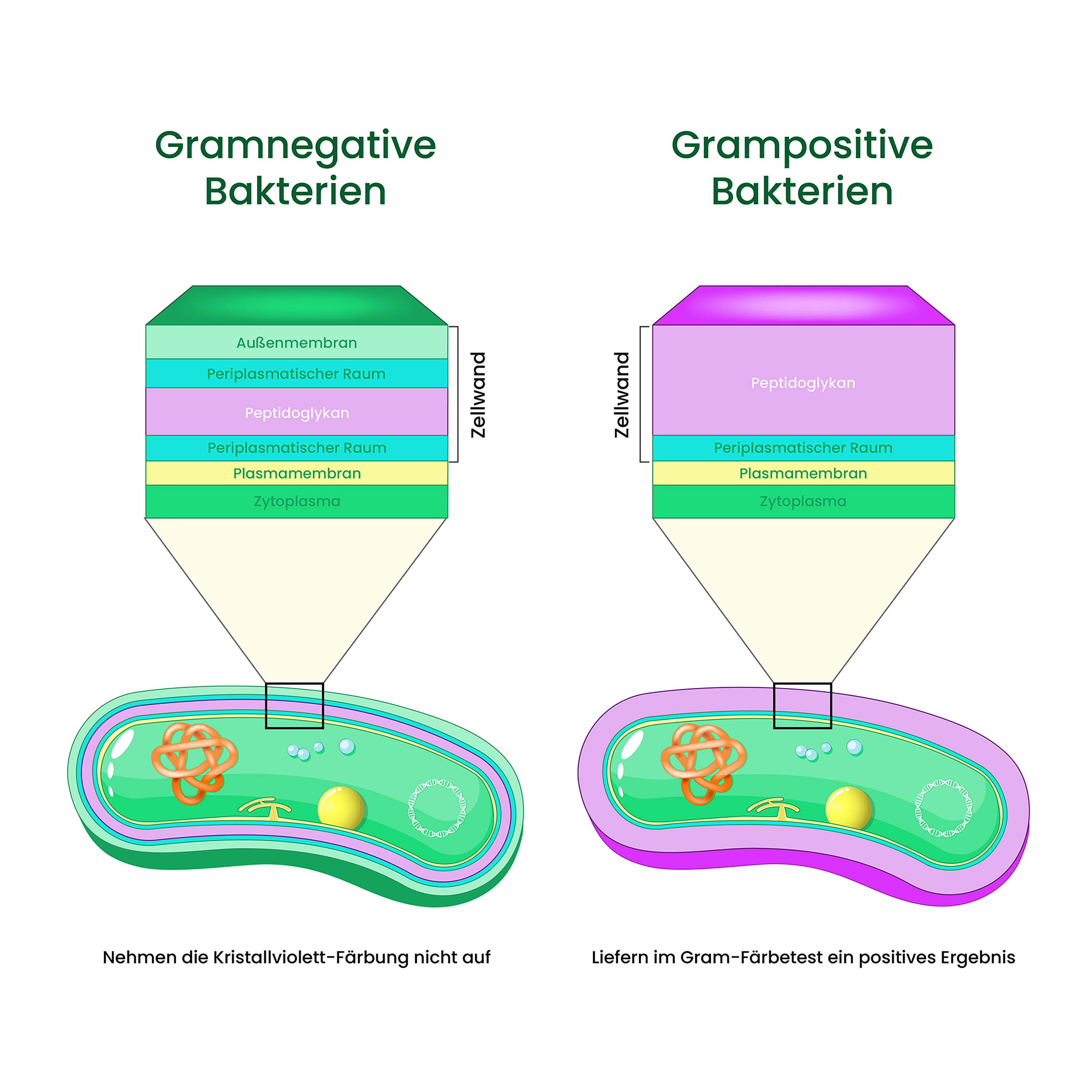
Bakterielle Zellwandstrukturen als PAMPs
Die Zellwände von Bakterien enthalten hochkonservierte Strukturen, die als PAMPs dienen und von PRR erkannt werden. Deren Architektur unterscheidet sich grundlegend bei grampositiven und gramnegativen Bakterien.
Grampositive Bakterien besitzen eine dicke Peptidoglykanschicht, die bis zu 40 Nanometer stark sein kann. In diese Schicht sind Teichonsäuren eingelagert, negativ geladene Polymere, die mit der Zellmembran verbunden sind. Lipoteichonsäuren durchspannen die gesamte Zellwand und verankern sich in der Zellmembran. Diese Strukturen liegen exponiert vor und sind direkt für Rezeptoren des Immunsystems zugänglich.
Gramnegative Bakterien haben eine komplexere Architektur. Über der Zellmembran liegt eine dünne Peptidoglykanschicht von nur 2 bis 7 Nanometern Dicke, darüber eine äußere Membran als zusätzliche Barriere. Diese äußere Membran enthält Lipopolysaccharid (LPS), das aus einem Lipid-A-Anteil, einer Core-Oligosaccharid-Region und einer O-Antigen-Kette besteht. LPS ist eines der potentesten PAMPs und löst bereits in minimalen Konzentrationen starke Immunreaktionen aus. Zwischen innerer und äußerer Membran befindet sich der periplasmatische Raum mit verschiedenen Enzymen und Transportproteinen.
Diese strukturellen Unterschiede erklären, warum das Immunsystem verschiedene Rezeptoren benötigt, um das gesamte Spektrum bakterieller Erreger zuverlässig zu erkennen.
Rezeptoren für Pathogenerkennung auf Makrophagen
Makrophagen exprimieren eine Vielzahl von Rezeptoren, die verschiedene bakterielle Strukturen erkennen. Diese Rezeptordiversität ermöglicht die Erkennung eines breiten Spektrums mikrobieller Erreger.
Der Mannoserezeptor ist ein Lektin, das terminale Mannose- und Fucose-Reste auf Oberflächen von Bakterien, Pilzen und Parasiten erkennt. Körpereigene Glykoproteine tragen typischerweise terminale Sialinsäuren statt Mannose – was die Unterscheidung zwischen Selbst und Fremd ermöglicht.
Der LPS-Rezeptor CD14 bindet Lipopolysaccharid gramnegativer Bakterien in Kooperation mit LPS-bindendem Protein aus dem Serum und dem Toll-like Receptor 4.
Toll-like Receptor 4 (TLR-4) ist der eigentliche Signaltransduktionsrezeptor für LPS. Nach Bindung von LPS an den CD14-LBP-Komplex interagiert dieser mit TLR-4 und dem Korezeptor MD-2, was intrazelluläre Signalkaskaden initiiert.
Toll-like Receptor 2 (TLR-2) erkennt Peptidoglykan und Lipoteichonsäuren grampositiver Bakterien sowie Lipoproteine. TLR-2 bildet Heterodimere mit TLR-1 oder TLR-6, wodurch die Ligandspezifität moduliert wird.
Der Glucanrezeptor Dectin-1 erkennt β-1,3-Glucane in Pilzzellwänden – Polysaccharide, die bei Bakterien und Säugetieren in dieser Form nicht vorkommen. Scavenger-Rezeptoren bilden eine heterogene Gruppe, die modifizierte Lipoproteine, apoptotische Zellen und verschiedene bakterielle Komponenten binden. Einige PRR, wie TLR-3, TLR-7 und TLR-9, befinden sich intrazellulär in Endosomen und erkennen dort Nukleinsäuren von Viren und Bakterien.