T-Zell-vermittelte Immunität
Die T-Zell-vermittelte Immunantwort ist besonders wichtig für die Bekämpfung intrazellulärer Erreger – also solcher, die sich in Körperzellen verstecken und dort der humoralen Immunantwort entziehen. T-Zellen koordinieren dabei sowohl die zelluläre als auch die humorale Abwehr und sind unverzichtbar für die Aktivierung von Makrophagen, B-Zellen und zytotoxischen Effektorzellen.
T-Zellen und intrazelluläre Erreger: Ein Fallbeispiel
Ein besonders anschauliches Beispiel für die T-Zell-vermittelte Immunität ist die Abwehr von Mykobakterien, zu denen auch der Tuberkulose-Erreger gehört. Diese Bakterien können innerhalb von Makrophagen überleben – genau jenen Zellen, die sie eigentlich vernichten sollten.
Wenn ein Makrophage Mykobakterien aufnimmt, kann er sie zunächst nicht abtöten. Der infizierte Makrophage präsentiert jedoch bakterielle Antigene auf MHC-Klasse-II-Molekülen. TH1-Zellen erkennen diesen Komplex und werden aktiviert. Die aktivierten TH1-Zellen schütten Interferon-γ aus – ein Zytokin, das den Makrophagen in einen hochaktiven Zustand versetzt und ihm die Kapazität gibt, die intrazellulären Bakterien nun doch zu vernichten. Dieses Zusammenspiel illustriert das Grundprinzip der T-Zell-vermittelten Immunität: nicht direktes Töten, sondern Aktivieren und Koordinieren anderer Effektorzellen.
Die drei Signale der T-Zell-Aktivierung
Für die vollständige Aktivierung einer naiven T-Zelle sind drei verschiedene Signaltypen notwendig, die von antigenpräsentierenden Zellen übermittelt werden.
Signal 1 ist die spezifische Antigenerkennung: Der T-Zell-Rezeptor (TCR) bindet an den Komplex aus Peptid und MHC-Molekül. Das CD4-Molekül auf der T-Zelle bindet gleichzeitig an MHC-Klasse-II und stabilisiert die Interaktion.
Signal 2 kommt von kostimulatorischen Molekülen: B7.1 und B7.2 (CD80/CD86) auf der antigenpräsentierenden Zelle binden an CD28 auf der T-Zelle. Ohne dieses zweite Signal wird die T-Zelle nicht vollständig aktiviert – ein wichtiger Schutzmechanismus gegen Autoimmunreaktionen.
Signal 3 besteht aus Zytokinen, die von der antigenpräsentierenden Zelle ausgeschüttet werden: IL-6, IL-12, TGF-β und andere. Diese Zytokine bestimmen, in welche Richtung sich die naive T-Zelle differenziert. Die Kombination aller drei Signale führt zur Aktivierung, zum Überleben und zur Differenzierung der T-Zelle in einen spezifischen Effektorzellentyp.
CD4-T-Zellen: Die Erkennungsspezialisten
CD4-T-Zellen, zu denen alle T-Helferzellen gehören, erkennen Antigene ausschließlich auf MHC-Klasse-II-Molekülen – die sich nur auf professionellen antigenpräsentierenden Zellen (dendritische Zellen, Makrophagen, B-Zellen) befinden. Nach Aktivierung können CD4-T-Zellen Makrophagen zur verstärkten Erregerabtötung aktivieren oder B-Zellen zur Antikörperproduktion stimulieren.
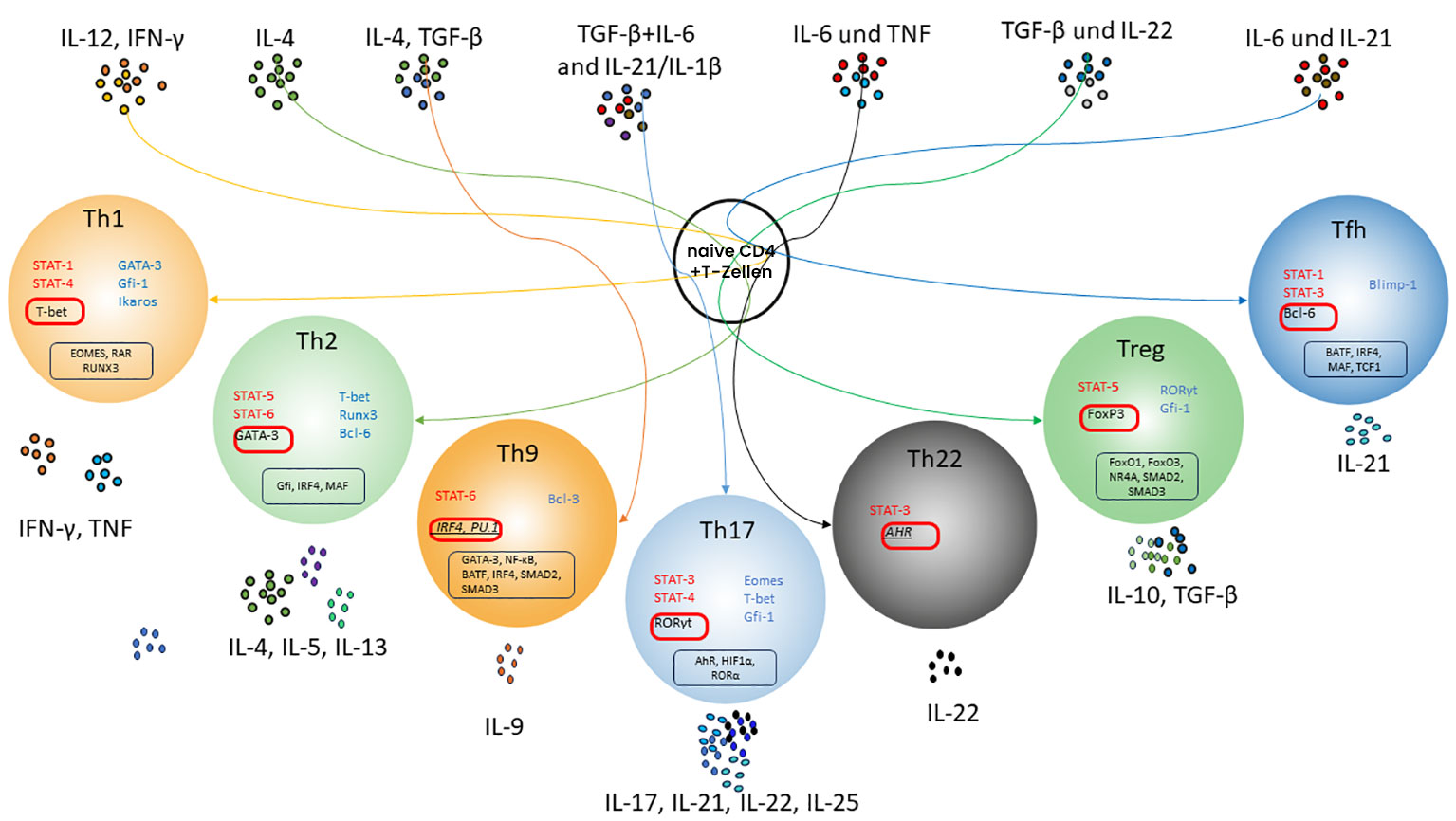
Die Vielfalt der T-Helferzellen
Abhängig von den Zytokinen des dritten Signals entwickeln sich naive CD4-T-Zellen zu verschiedenen Subtypen mit unterschiedlichen Spezialisierungen:
TH1-Zellen entstehen durch IL-12 und Interferon-γ (Transkriptionsfaktor T-bet). Sie produzieren IL-2 und Interferon-γ und sind spezialisiert auf die Abwehr intrazellulärer Erreger wie Mykobakterien, Listeria, Leishmania und Pneumocystis sowie extrazellulärer Bakterien.
TH2-Zellen entstehen unter IL-4-Einfluss (Transkriptionsfaktor GATA-3). Sie produzieren IL-4 und IL-5 und sind auf die Bekämpfung parasitischer Helminthen spezialisiert. Sie unterstützen B-Zellen besonders beim Klassenwechsel zu IgE-Antikörpern.
TH17-Zellen entstehen durch TGF-β und IL-6 (Transkriptionsfaktor RORγT). Sie produzieren IL-17 und verstärken die Rekrutierung neutrophiler Granulozyten – wichtig bei der Abwehr extrazellulärer Bakterien wie Salmonella enterica.
Regulatorische T-Zellen (Tregs) entstehen unter TGF-β und IL-10 (Transkriptionsfaktor FoxP3). Sie produzieren selbst TGF-β und IL-10 und dämpfen überschießende Immunreaktionen – ihre Hauptaufgabe ist das Verhindern von Autoimmunität.
TR1/TH3-Zellen entstehen ebenfalls durch IL-10 und TGF-β und wirken regulatorisch, ihr Transkriptionsfaktor ist noch nicht vollständig charakterisiert.
Diese Differenzierung zeigt, wie das Immunsystem seine Reaktion präzise auf die Art der Bedrohung abstimmt.
T-Effektorzellen im Überblick
Zytotoxische CD8-T-Zellen (CTL) töten virusinfizierte Zellen und Zellen mit intrazellulären Bakterien ab – sie erkennen ihre Ziele über MHC-Klasse-I-Moleküle auf allen kernhaltigen Zellen. CD4-TH1-Zellen aktivieren infizierte Makrophagen und unterstützen B-Zellen bei der IgG-Produktion. CD4-TH2-Zellen fördern den Antikörper-Klassenwechsel zu IgE für die Parasitenabwehr. CD4-TH17-Zellen rekrutieren Neutrophile gegen extrazelluläre Bakterien. Regulatorische CD4-T-Zellen bremsen überschießende Reaktionen.
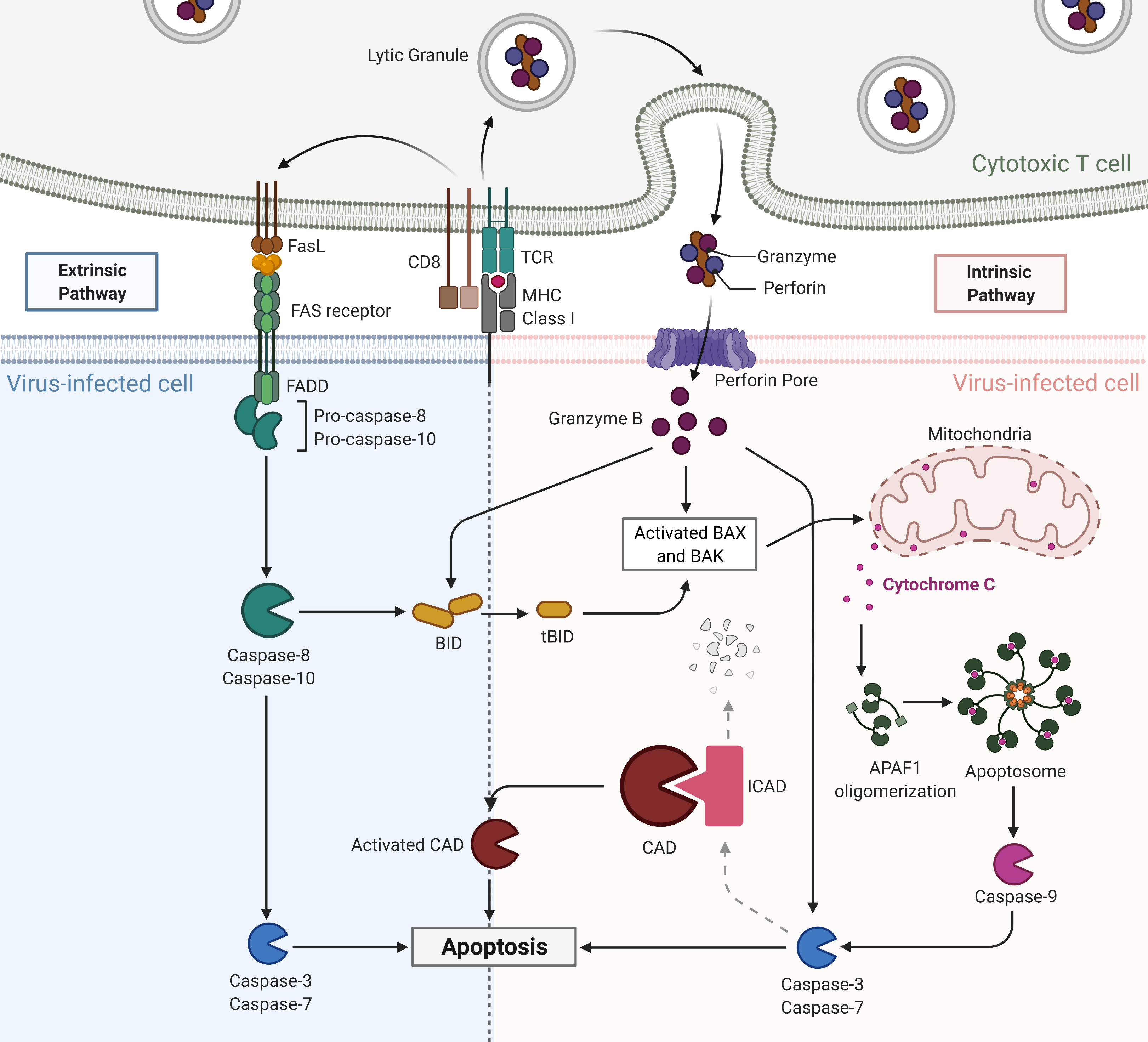
Zytotoxische T-Zellen: Die Killer des Immunsystems
Zytotoxische CD8-T-Zellen erkennen über ihren T-Zell-Rezeptor den Komplex aus einem viralen oder bakteriellen Peptidfragment und einem MHC-Klasse-I-Molekül auf der Oberfläche einer infizierten Zelle. Das CD8-Molekül bindet zusätzlich an MHC-Klasse-I und stabilisiert die Interaktion.
Sobald die zytotoxische T-Zelle ihre Zielzelle erkannt hat, setzt sie zytotoxische Granula frei, die Perforin und Granzyme enthalten. Perforin bohrt Löcher in die Membran der Zielzelle, durch die Granzyme eindringen. Diese Enzyme aktivieren in der Zielzelle das Apoptoseprogramm: Die Zelle stirbt kontrolliert ab, ohne ihren Inhalt freizusetzen – was Entzündungen minimiert und verhindert, dass Viren aus der sterbenden Zelle entweichen und weitere Zellen infizieren.
Die zytotoxische T-Zelle tötet die Zielzelle nicht direkt, sondern bringt sie dazu, Selbstmord zu begehen. Nach diesem Vorgang löst sie sich und kann weitere infizierte Zellen attackieren.